____________________________________________
Hernri AZAÏS : Assistance Publique des Hôpitaux de Paris (AP-HP), Hôpital Européen Georges Pompidou, service de chirurgie cancérologique gynécologique et du sein, Paris, France.
Marianne NIKPAYAM et Catherine UZAN : Assistance Publique des Hôpitaux de Paris (AP-HP), Hôpital Pitié-Salpêtrière, service de chirurgie et oncologie gynécologique et mammaire, Paris, France.
____________________________________________
De nouvelles technologies sont maintenant à la disposition des praticiens pour le repérage des lésions du sein et du ganglion sentinelle axillaire [1]. Le dépistage permet en effet la découverte de cancers du sein à un stade infra clinique, c’est-à-dire non palpable, et un repérage est indispensable pour guider le chirurgien pour leur exérèse chirurgicale.
On peut citer les systèmes suivants :
- Celui développé par SYSMEX repose sur les propriétés de marqueurs ferromagnétiques. Le système Magseedâ est un clip ferromagnétique, mis en place au sein de la tumeur avant l’intervention et qui permet de repérer la lésion lors de la chirurgie à l’aide d’une sonde (Sentimagâ : figure 1). On peut implanter le clip sans contrainte de délai entre la pose et la chirurgie sous réserve de prévoir de le retirer, ce qui permet de repérer les lésions avant chimiothérapie néoadjuvante. Les avantages mis en avant par le fabricant sont pour le clip, l’absence de fil externe, la flexibilité de l’organisation entre le radiologue et le chirurgien pour la programmation de l’intervention, la possibilité de repérer le clip par mammographie ou échographie (figure 2). Pour la patiente, le dispositif serait également moins douloureux, à l’origine de moins d’appréhension, alors que pour le chirurgien profiterait d’un repérage plus précis qu’avec un guide traditionnel (figures 3 et 4).
La détection du ganglion sentinelle axillaire est également possible avec la sonde Sentimagâ et le traceur Magtraceâ (figure 5) qui peut être injecté dans le sein avant la date programmée de l’opération avec également le confort de la flexibilité et de la simplification du parcours de soin mais également l’intérêt de ne pas avoir recours à l’utilisation d’un produit radioactif et de pouvoir se soustraire aux contraintes liées à la médecine nucléaire.
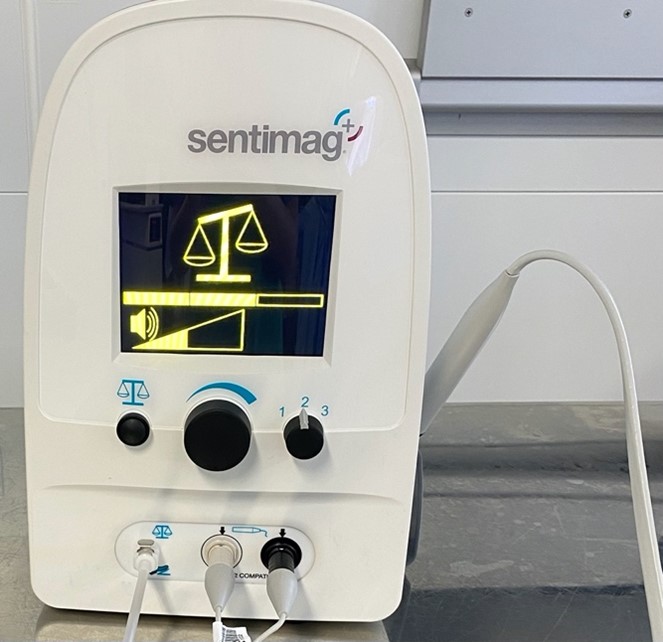
Figure 1 : sonde Sentimag
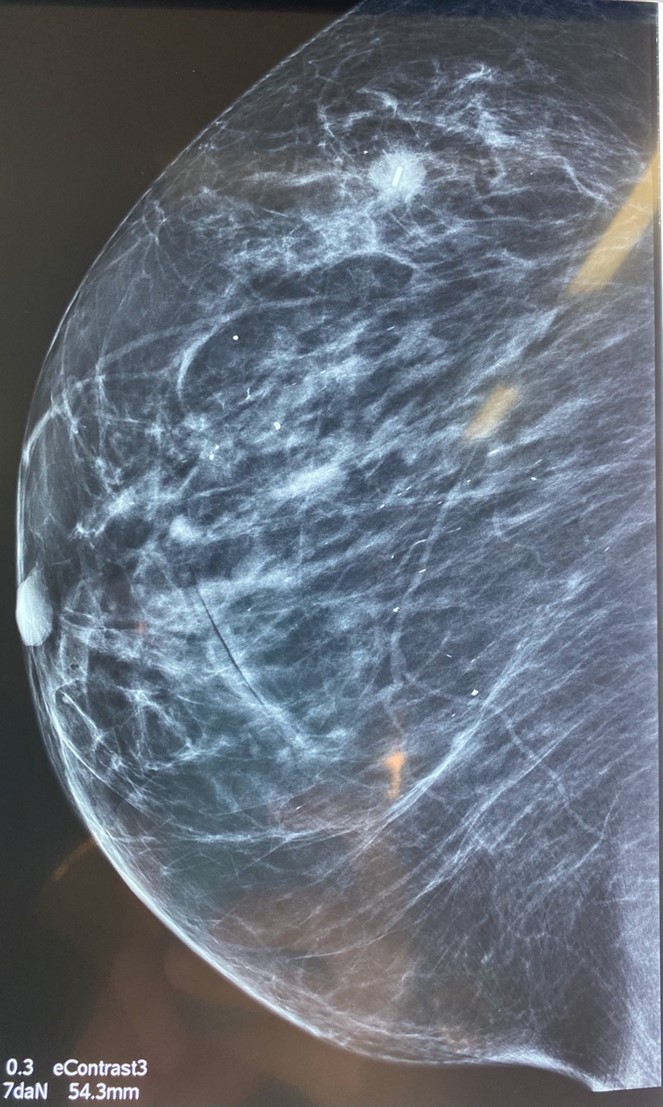
Figure 2 : Repérage pré opératoire : mise en place d'un clip
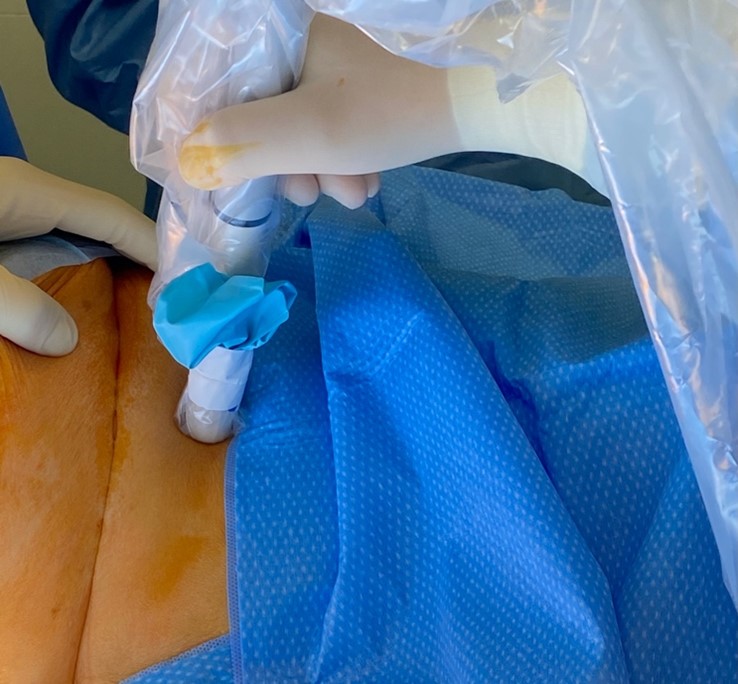
Figure 3 : localisation per opératoire du clip par la sonde Sentimag
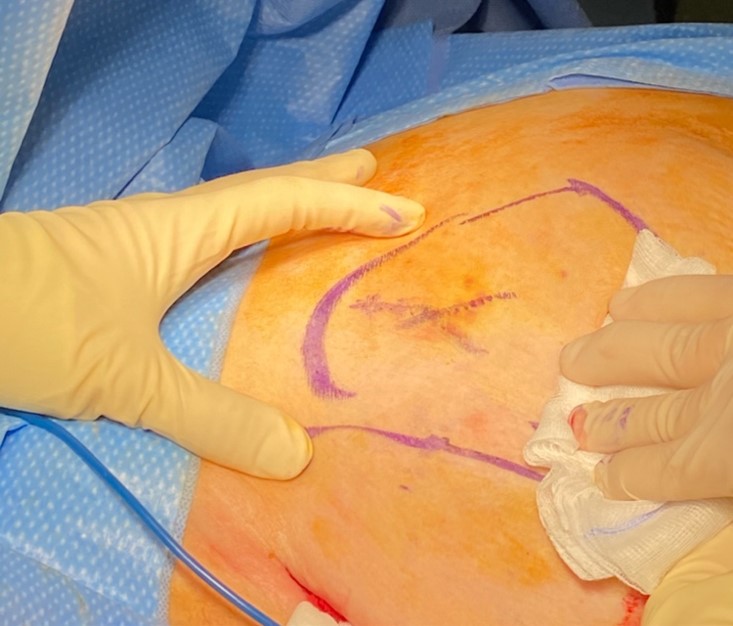
Figure 4 : marquage cutané du site après repérage par la sonde Sentimag
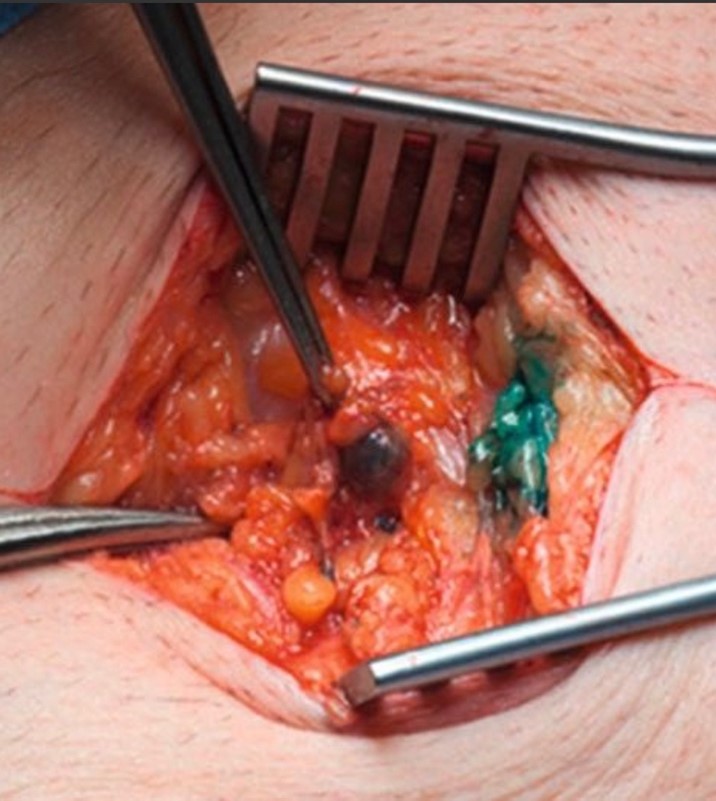
Figure 5 : repérage du ganglion sentinelle par le traceur Magtrace
- La technologie SAVI SCOUTâ repose sur les propriétés d’un réflecteur mis en place au cœur de la lésions dont on souhaite réaliser l’ablation (ganglion ou tumeur du sein). Ici, c’est un système radar qui permet de détecter la présence du matériel. Celui-ci peut être mis en place avant l’intervention, sous guidage radiologique, avec les mêmes avantages qu’avec les marqueurs ferromagnétiques, en particulier moins de douleurs, l’absence de fil externe et une plus grande facilité d’organisation du parcours de soins, sans pour autant conduire à un taux supérieur de berges chirurgicales atteintes [2].
- La technologie du grain d’iode 125 (IsoSeedâ - Eckert & Ziegler) permet également de repérer des tumeurs mammaires non palpables. Le repère utilisé mesure 0,8 mm × 4,5 mm et émet un rayonnement gamma. Dans l’étude publiée par Hoog et al., il est indiqué que le grain d’iode est mis en place en radiologie sous contrôle échographique ou mammographique jusqu’à 10 jours avant la chirurgie. Le repérage du ganglion sentinelle est réalisé la veille ou le jour même par nanocolloïdes marqués au 99mTc. Le grain est radio-opaque et échogène. Dans cette étude menée sur 116 patientes. Soixante repérages par harpon et 56 repérages par grain d’iode ont été réalisés. Cinquante grains ont été placés sous échographie et six sous mammographie. Les durées de mise en place radiologique et de l’acte opératoire sont réduites avec le grain d’iode (p< 0,03). Le taux de reprise chirurgicale est identique. L’inconfort évalué par échelle EVA est identique lors de la pose du repère et inférieur dans le cas du grain 3 à 24 heures après le geste radiologique (p< 0,003). La présence simultanée de 99mTc et de 125I n’a pas d’influence sur la détection d’un ganglion sentinelle ou d’une lésion repérée par grain. Cette technique multidisciplinaire est jugée faisable par les auteurs [3]. Un des désavantages de cette approche par rapport à celles discutées précédemment et la persistance des contraintes liées à la détection du ganglion sentinelle en lien avec les services de médecine nucléaire qui alourdissent l’organisation du parcours des patientes.
Le prix reste un frein à la diffusion de ces systèmes de détection de nouvelle génération, et il convient de poursuivre les études cliniques afin de confirmer leur fiabilité. Néanmoins, les avantages avancés, en particulier le confort des patientes et la simplification des parcours et des organisations sont de réels arguments pour s’intéresser à leurs applications. La désescalade attendue dans les indications de chirurgie ganglionnaire axillaire, l’augmentation des indications de chimiothérapie néoadjuvante, pourraient, elles aussi, contribuer à l’essor de ces technologies avec la possibilité de repérer les tumeurs et ganglions métastasiques avant chimiothérapie pour et permettre ainsi leur exérèse élective lors du temps chirurgical [4].
Références
1. Norman C, Lafaurie G, Uhercik M, Kasem A, Sinha P. Novel wire-free techniques for localization of impalpable breast lesions-A review of current options. Breast J 2021;27(2):141‑8.
2. Srour MK, Kim S, Amersi F, Giuliano AE, Chung A. Comparison of Multiple Wire, Radioactive Seed, and Savi Scout® Radar Localizations for Management of Surgical Breast Disease. Ann Surg Oncol 2021;28(4):2212‑8.
3. Hoog C, Gal J, Dejean C, Chapellier C, Dejode M, Delpech Y, et al. Résultats intermédiaires de l’étude comparant la technique du grain d’iode 125 à celle du harpon dans le repérage des tumeurs mammaires non-palpables. Médecine Nucléaire 2019;43(2):214.
4. Laws A, Dillon K, Kelly BN, Kantor O, Hughes KS, Gadd MA, et al. Node-Positive Patients Treated with Neoadjuvant Chemotherapy Can Be Spared Axillary Lymph Node Dissection with Wireless Non-Radioactive Localizers. Ann Surg Oncol 2020;27(12):4819‑27.
A lire aussi sur Gynéco-Online
Détection des lésions non palpables du sein par grain d’iode. Professeur Emmanuel Barranger.





